Идентификация генов, кодирующих ферменты биосинтеза эктоина у M.marinaСтраница 1
Для идентификации генов синтеза эктоина у M. marina был использован подход, основанный на ПЦР методологии. Проведенный ранне анализ опубликованных и представленных в GenBank данных свидетельствовал о том, что у исследованных видов галофильных и галотолерантных бактерий гены, кодирующие ДАБ-ацетилтрансферазу, ДАБ-аминотрансферазу и эктоинсинтазу, расположены в одном кластере в последовательности ectABC. В результате сравнения аминокислотных последовательностей этих белков у галофильных гетеротрофных бактерий Marinococcus halofilus DSMт20408, Halomonas elongatа DSM 2581, Cromohalobacter salexigens (ранее Halomonas elongatа DSM 3043), Bacillus pasteurii, Vibrio cholerae, Bacillus haldurans, Oceanobacillus iheyensis (GenBnk AP004594), Streptomyces coelincolor (GenBank AL591322), а также ectABC кластеров у метилотрофных бактерий (Mm. alcaliphilium 20Z, Mm. kenyense AMO1, M. alcalica M8 и M. thalassica MT), и анализа найденных гомологичных участков были выбраны наиболее консервативные последовательности. С учётом вырожденности и встречаемости кодонов в генах, кодирующих эти белки, мы использовали ранее разработанные и созданные новые вырожденные праймеры для их амплификации (Рис. 5). При конструировании праймеров предполагалось, что у M. marina гены биосинтеза эктоина находятся в одном кластере и расположены последовательно: ectA, ectB и ectC (Рис. 5).
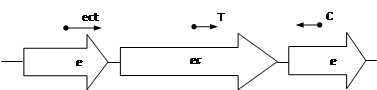
Рис. 5. Схема расположения генов биосинтеза эктоина у M. marina и разработанных вырожденных праймеров (ectHal, Tra3, CR).
Нуклеотидные последовательности праймеров ectHal и Tra3-CR представлены в табл. 5.
C использованием пары праймеров Tra3-CR были получены ПЦР-фрагменты генов ectB и ectC общей длиной ~1000 п.н. (Рис. 5а). ПЦР-продукт клонировали в вектор рZero и секвенировали. На основе выявленной нуклеотидной последовательности был синтезирован праймер HalR, комплементарный этой последовательности. С использованием вырожденного праймера ectHal и HalR был получен ПЦР-продукт длиной ~1150 п.н. содержащий 3’-конец гена ectA и 5’-конец гена ectB (Рис. 5б). Это указывало на сопряженное расположение генов в кластере в первоначально предположенной последовательности – ectABC. Допуская, что, аналогично другим метилотрофам - Mm. alcaliphilium 20Z, M. alcalica M8 и M. thalassica MT (Решетников, 2006), вслед за геном ectC расположен ген, кодирующий специфическую аспартаткиназу, был сконструирован и синтезирован вырожденный праймер Rtn на ген ask. С использованием комплементарного праймера HalF на ген ectB и вырожденного праймера Rtn был амплифицирован фрагмент ДНК длиной ~1250 п.н. и секвенирован (Рис. 6с)
Таким образом, мы получили полные последовательности генов ectB и ectC, а также ~100 п.н. гена ectA и ~180 п.н. гена ask.
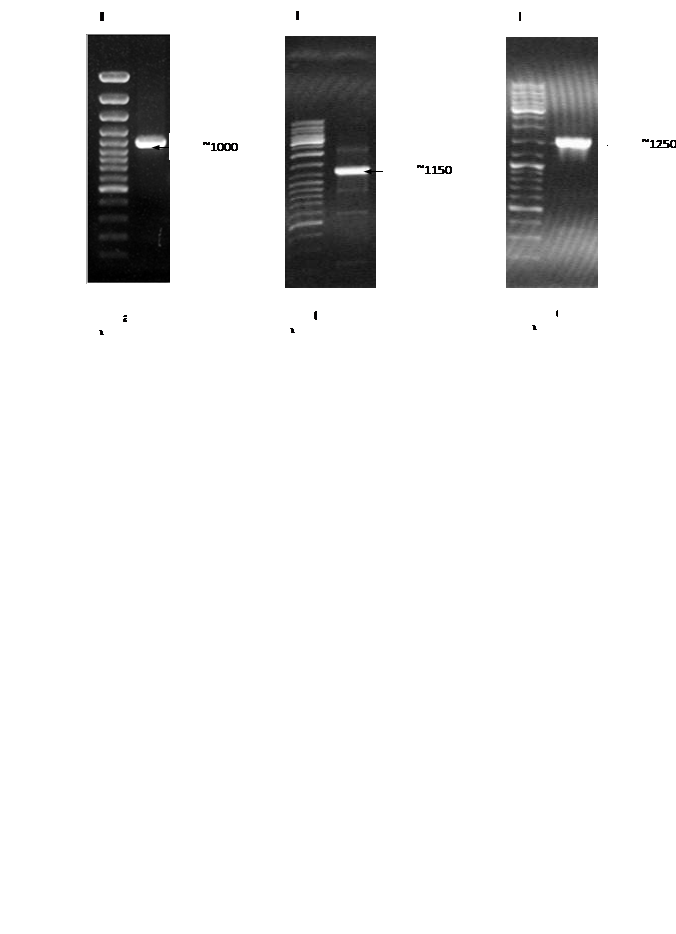
Рис. 6. Электрофорез ПЦР продуктов полученных с использованием праймеров:
a) Tra3-CR; б) ectHal-HalR и c) HalF-Rtn. M - маркер “ Gene RulerTM 100bp DNA Ladder plus”.
Секвенирование ПЦР-продуктов и анализ нуклеотидных последовательностей позволили объединить их в один фрагмент длиной ~2100 п.н., в котором обнаружены четыре открытые рамки считывания, среди которых ОРС, соответствующие генам ectA и ask, были неполными.
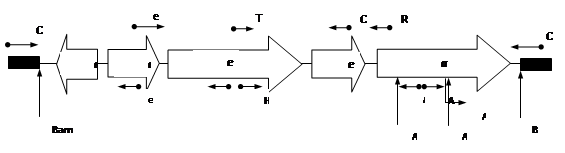
Рис. 7. Схема расположения ect-генов у M. marina и положение праймеров. Последовательности праймеров приведены в табл. 5.
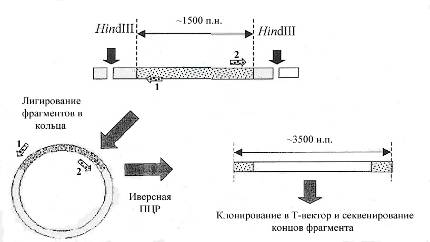
Для идентификации недостающей последовательности гена ask была применена стратегия инвертированной ПЦР. Инвертированная (от англ. “inverse”), или обратная, ПЦР применяется для клонирования областей ДНК, непосредственно прилегающих к области с известной последовательностью. Данный подход удобен тем, что устраняется необходимость создания геномных библиотек и их последующего скрининга, что достаточно трудоёмко. Суть метода заключается в следующем: геномную ДНК фрагментируют расщеплением эндонуклеазами, не имеющими сайтов внутри известной последовательности. Полученные фрагменты лигируют при низкой концентрации ДНК в условиях, когда образуются преимущественно кольцевые молекулы. Полученные кольцевые молекулы ДНК используют в качестве матрицы в ПЦР, которую проводят с праймерами (Рис. 8, праймеры 1 и 2), соответствующими концевым областям известной последовательности, синтез с которых направлен в стороны с неизвестной последовательностью (Sambrook, Russell, 2001).
|
Также смотрите:
Органы, полости тела и нервная система земноводных
Особенности внутреннего строения. У земноводных в отличие от рыб развились слюнные железы. Зубы, если имеются, конической формы и способствуют удерживанию добычи. У многих хвостатых конец языка обращен назад и при ловле насекомых может выбрасываться далеко вперед. Жел ...
Приложения
Приложение 1
Биотопическое распределение насекомых на территории парка и экологическая характеристика встреченных видов.
№
виды
(78 вида)
Лесной биотоп
(39 видов)
Лугово-степной биотоп
(58 видов)
Околоводный биотоп
(27 видов)
Экологическая хара ...
Общая характеристика "тела" планеты Земля
Ещё в XIX столетии стало ясно, что у Земли должно быть плотное ядро. Действительно, плотность наружных пород земной коры составляет около 2800 кг/м3 для гранитов и примерно 3000 кг/м3 для базальтов, а средняя плотность нашей планеты - 5500 кг/м3. В то же время существ ...